급성췌장염으로 발현한 췌관내유두상점액종양 연관 침습암 1예
Intraductal Papillary Mucinous Neoplasm with an Associated Invasive Carcinoma Manifested by Acute Pancreatitis
Article information
Abstract
급성 췌장염 중에 1차 검사에서 원인이 불명확한 경우 급성 특발성 췌장염이라고 하며 그 중 종양에 의한 것은 비교적 드물지만 진단이 늦어질 경우 예후가 좋지 않아 먼저 의심하는 것이 매우 중요하다. 본 증례는 급성 특발성 췌장염 환자에서 악성종양을 의심하고 적극적으로 추적관찰하던 과정에서 초음파내시경상 이상소견이 확인되었고, 적절한 시기에 수술을 결정하여 췌관내유두상점액종양 관련 침습암을 진단한 경우이다. 따라서 원인이 불분명한 췌장염에 대해 악성종양을 의심하는 것이 필요함을 강조함과 동시에 초음파내시경의 추적관찰이 진단에 도움이 된 실제 사례를 보고함으로써 앞으로의 진료 및 의사결정에 유익할 것으로 보여 문헌과 함께 보고하는 바이다.
Trans Abstract
Idiopathic acute pancreatitis (IAP) is defined as acute pancreatitis for which the standard initial evaluation has failed to reveal the etiology. Although a tumor is a rare cause of IAP, it is important to consider it in advance, because prognosis is poor if diagnosis is delayed. We describe a case of presumed IAP at the index presentation that was finally diagnosed as intraductal papillary mucinous neoplasm with an associated invasive carcinoma in a 70-year-old woman after surgery to remove a mass identified during follow-up endoscopic ultrasonography. Therefore, this is a case in which suspicion of malignancy and follow-up endoscopic ultrasonography helped to appropriately diagnose and treat the tumor.
서 론
급성 췌장염은 췌장과 췌장 주위 조직의 염증이 발생하는 질환으로 국소적인 염증반응뿐만 아니라 전신적 염증반응까지 발생할 수 있으며 심한 경우 다기관부전까지도 발생하여 약 10%의 비교적 높은 사망률을 보인다[1]. 최근 급성 췌장염의 발생률이 증가하고 있으며 그 원인으로는 담석이 45%, 알코올이 35%로 가장 흔하다고 알려져 있다[2].
대부분 병력 및 1차 검사에서 원인이 발견되나, 그렇지 않은 경우 특발성 췌장염이라 하며 이러한 경우에는 재발 가능성이 있으므로 원인을 찾기 위해 노력해야 한다. 특발성 췌장염의 원인으로 미세결석, 오디괄약근 기능장애, 분할췌, 선천성 췌장염, 낭성 섬유증, 담관낭종, 비정상적 담췌관 연결부위, 윤상췌장, 췌담도암, 만성 췌장염 등이 있다[3]. 원인이 악성종양인 경우는 비교적 드물지만, 악성종양의 진단이 늦어질 경우 문제가 될 수 있으므로 췌장염이 발생하였을 때 원인이 불명확하다면 악성종양이 원인이 아닌지 한번쯤은 생각해 볼 필요가 있다. 본 증례는 급성 췌장염이 발생하였으나 그 원인이 불명확하여 경과관찰 하던 중 시행한 초음파내시경에서 발견된 췌장의 악성종양에 대해서 수술적 절제를 시행하여 치료한 증례로 원인이 불명확한 췌장염에서 악성종양을 의심하여 진단 및 수술 결정에 도움을 주었기에 증례 보고하는 바이다.
증 례
70세 여성이 과식 후에 발생한 복통을 주소로 타병원 방문 후 췌장효소수치 상승이 확인되고, 영상검사에서 췌장의 미만성 염증소견이 확인되어 급성 췌장염 진단을 받아 치료를 받았다. 당시 복부영상검사에서 췌관의 이상이 관찰되어 추가 평가를 위해 본원 내원하였다.
당뇨 외에 특이한 과거병력은 없었으며, 흡연 및 음주력은 부인하였고 가족력에서 특이사항은 없었다. 전신 쇠약감 및 체중감소는 없었으며, 발열 및 오한, 복통, 구역, 구토 등의 증상은 없었다.
의식은 뚜렷하고 지남력은 명료하였으며 혈압은 116/70 mmHg, 맥박은 분당 68회, 호흡수는 분당 18회, 체온은 37℃였다. 공막에 황달은 보이지 않았고 복부는 편평하였으며 장음은 정상적이었다. 복부 종괴는 촉지되지 않았으며 압통 및 반발통도 없었다. 간, 비장, 신장은 촉지되지 않았다.
말초혈액 검사에서 백혈구 9,860/mm3, 혈색소 14.4 g/dL, 혈소판 160,000/mm3이었고, 간기능 검사에서 총콜레스테롤 139 mg/dL, 총단백 6.8 g/dL, 알부민 3.9 g/dL, 총 빌리루빈 1.6 mg/dL, 알칼리성 인산분해효소 58 IU/L, 아스파탐산아미노전이효소와 알라닌아미노전이효소는 19/15 IU/L, 감마글루타밀전이효소는 17 IU/L이었다. 혈청 아밀라아제 97 U/L, 혈청 리파아제 66 U/L, 프로트롬빈시간은 78% (INR 1.20)이었다. 종양표지자 검사에서 carcinoembryonic antigen (CEA)은 2.8 ng/mL, carbohydrate antigen 19-9 (CA19-9)는 135 U/mL이었다.
타병원 내원 당시 시행한 복부 전산화단층촬영에서는 췌장 두부를 중심으로 전반적인 부종 및 주변의 지방침윤으로 급성 췌장염에 합당한 소견과 주췌관의 미세한 확장이 관찰되었으며, 자기공명영상에서는 주췌관이 췌장 미부에서 좁아지면서 미부쪽의 낭성확장 또는 낭성병변과의 연결을 보이고 있었다(Fig. 1). 본원 내원 이후 초음파내시경을 시행하였으나 당시 췌장실질의 이상은 관찰되지 않았다. 3개월 후 시행한 복부 전산화단층촬영에서도 여전히 췌관의 협착이 관찰되어 내시경적 역행성담췌관조영술을 시행하였다. 검사에서 원위부 췌관의 협착이 관찰되고 췌관 미부는 조영이 되지 않는 소견을 보여, 추후 췌장염 재발 방지를 위해 췌관 내 플라스틱 스텐트를 삽입하였다 (Fig. 2). 당시 CA19-9 수치는 처음보다 감소하여 20 U/mL이었으며 추적관찰 중에도 더 이상 증가하지 않았다.

(A) An abdominal CT image shows edema around the head of the pancreas and peripancreatic fat infiltration, which are typical radiologic findings of acute pancreatitis.(B) An MRI scan reveals abrupt narrowing of the pancreatic duct at the tail-body junction with upstream cystic dilatation in the tail of the pancreas(arrow).
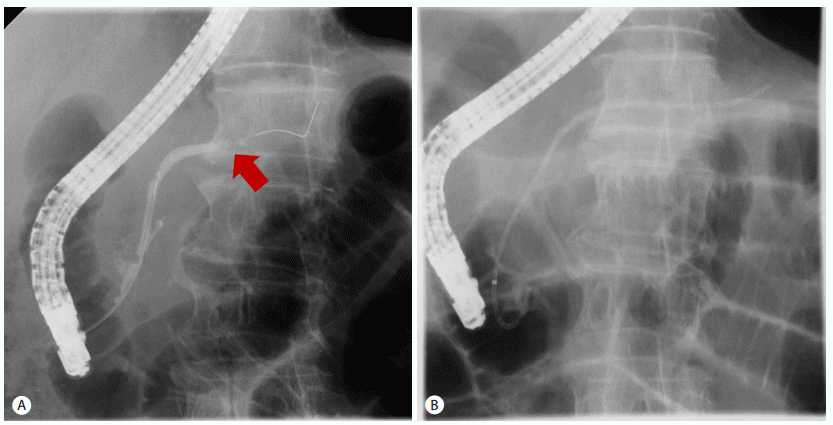
(A) ERCP illustrates an area in the pancreatic tail duct without contrast filling due to a stenosis at the pancreas body-tail duct (arrow).(B) A plastic stent was inserted to resolve the stenosis.
이후 복통 재발 없이 경과관찰하였고 3개월 후 시행한 복부 전산화단층촬영에서 췌관 스텐트는 빠져있고 여전히 췌관 체미부 연결부위가 좁아져 있으며, 그 상부로 낭성병변이 이전과 거의 변화 없는 상태로 보였다. 지속되는 췌관 협착에 대한 정확한 평가 및 악성종양 감별을 위해 초음파내시경을 다시 시행하였고, 췌장 체미부에 약 2 cm 크기의 저에코성의 병변이 관찰되었다(Fig. 3).

Abdominal CT performed 3 months later reveals the remaining (A)abrupt narrowing of the pancreatic duct at the tail-body junction (arrow) with (B)upstream cystic dilatation in the tail of the pancreas (arrow).(C)An EUS image illustrates a 2-cm hypoechoic mass at the body of the pancreas.
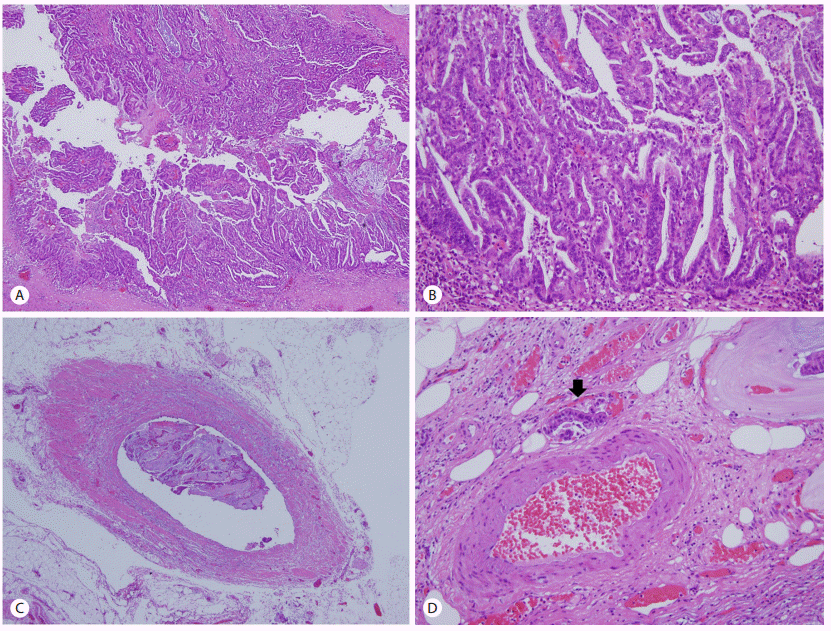
내시경적인 치료만으로는 협착이 해결될 수 없어 추후 췌장염이 재발할 가능성이 있고, 초음파내시경에서는 전산화단층촬영에서 보이지 않던 저에코성 병변이 관찰되어 악성 종양이 의심되었으므로 이후 외과와 상의 하에 원위췌장절제술(distal pancreatectomy)을 시행하였다(Fig. 4). 수술 후 병리검사 상 췌장 체미부에 4.8×2.0×1.3 cm 크기의 종괴가 발견되었고, 주췌관 및 분지췌관을 모두 침범하고 있으며 유두상 성장을 보이고 있어 혼합형 췌관내유두상점액종양에 합당한 소견이었다. 90% 이상에서 침습암종이 관찰되며, 고배율로 관찰시 중등도 분화도를 보였다(Fig. 5). 종괴는 췌장 주위 연조직까지 침범하였지만 복강 축 및 상장간동맥의 침범은 없었고 림프절 총 7개 중에 1개에서 전이가 발견되어 최종 pT3N1의 췌관내유두상점액종양 연관 침습암으로 진단되었다.

Gross specimen examination after distal pancreatectomy showed that the main pancreatic duct was dilated at the upstream portion of the stenosis. A 2-cm mass was observed inside the dissected main pancreatic duct.
고 찰
본 증례는 복통을 주소로 내원한 70세 여성에 대한 증례로 원인이 명확하지 않은 급성췌장염으로 추적관찰 하던 중 초음파내시경에서 췌장 체미부에 저에코성 병변이 발견되어 악성종양 의심 하에 수술 후 췌관내유두상점액종양 연관 침습암으로 진단된 증례이다.
보통 처음으로 췌장염 발생시 1차적인 검사 결과 70-90%에서 그 원인을 찾을 수 있다고 알려져 있는데, 1차 검사로는 알코올, 약물, 가족력에 대한 병력청취와 혈중칼슘농도, 중성지방, 간기능검사 등의 혈액검사와 복부초음파 또는 전산화단층촬영 등의 영상검사를 시행한다. 1차 검사에서 그 원인을 찾지 못하는 비율이 10-30%로 이러한 경우를 특발성 췌장염이라고 하며 그 원인 중 췌담도 종양은 양성 및 악성을 포함하여 5-7%로 비교적 드문 원인에 해당한다[3].
이는 크게 췌장암, 낭성종양, 팽대부종양으로 나눌 수 있으며 낭성종양, 팽대부종양의 경우에는 양성 종양일 가능성도 있으나 그 감별이 쉽지 않고 전암성 병변일 가능성이 있어 악성종양을 배제할 수 없기 때문에 수술을 결정하게 되는 경우가 많다. 그러나 최근 보고된 증례들을 보았을 때 특발성 췌장염에서 보이는 종괴에 대해 악성종양의 가능성으로 수술을 결정하였으나 최종 병리검사 결과에서 양성질환으로 보고되는 경우가 늘어나고 있고 Whipple 수술 같은 경우 수술 자체로 인한 합병증 및 위험성을 동반하고 있어 수술 전 양성과 악성의 감별이 매우 중요시되고 있다[4-6]. 종양 이외에도 자가면역성 췌장염에서는 최대 27%에서 췌장암과 비슷한 형태의 종양으로 발견되어 수술을 받았다고 하여 췌장암으로 인한 급성 특발성 췌장염이 의심될 때 감별이 필요하다[7,8].
본 증례에서는 췌관내유두상점액종양 관련 침습암으로 인해 급성 특발성 췌장염이 발생한경우이며, 췌관 내로 점액을 분비하여 췌관을 막았거나, 종양에 의해 췌관의 협착이 발생하였기 때문으로 생각된다[9]. 이 경우 종양이 있는 부위와는 다른 곳에서 췌장염이 발생할 수 있고 낭성종양 자체가 급성 췌장염 이후의 가성낭종과 감별이 쉽지 않아 췌장염의 원인을 밝히기 어렵기 때문에 처음에 진단이 늦어질 수 있다[10]. 췌관내유두상점액종양은 주췌관형, 부췌관형, 혼합형으로 나눌 수 있다. 주췌관 직경이 5 mm 이상으로 늘어나 있는 경우를 주췌관형이라 하며 부췌관형은 췌장낭종의 크기가 5 mm 이상이면서 주췌관과 교통이 되어 있는 경우이고 혼합형은 주췌관형과 부췌관형의 조건을 모두 만족시키는 경우이다[11]. 그중에서 주췌관형은 60%에서 악성위험성이 있고 부췌관형에서는 췌장두부의 낭성 병변이 폐쇄성 황달을 일으키거나 주췌관 직경이 10 mm 이상 혹은 낭종 내 조영증강되는 고형성 병변이 있는 경우 악성위험성이 높아 수술을 권장한다[11]. 본 증례는 최종적으로 혼합형 췌관내유두상점액종양으로 확진되었으나, 수술 전 전산화단층촬영 및 자기공명영상에서 췌관의 낭성확장인지 낭성종양인지 감별이 어려웠고, 초음파내시경 시행 전까지는 고위험 stigmata가 없었기 때문에 바로 수술하지 않았다[11].
급성 특발성 췌장염에서 원인을 감별하기 위한 추가적인 검사로 내시경적역행성췌담관조영술, 초음파내시경, 자기공명췌담관조영술 등을 시행할 수 있으며 그 중에 최근 민감도와 안전성으로 인해 초음파내시경의 중요성이 점차 증가하고 있다[3]. 초음파내시경은 전산화단층촬영이나 자기공명영상보다 해상도가 높아 췌장실질을 더욱 잘 관찰할 수 있으므로 최근 췌장암의 병기결정에 전산화단층촬영보다 정확하다는 보고가 있으며, 특히 2 cm 미만의 병변에 대해 더 정확히 진단할 수 있다[12]. 낭성병변의 관찰이 용이하고 본 증례처럼 췌장내유두상점액종양의 경우 벽결절의 평가를 통해 악성화의 가능성을 예상할 수 있으며[13], 세침흡인검사를 통해 더 정확한 진단을 할 수 있는 장점이 있다[14]. 이러한 점에서 췌장염의 원인이 불명확할 경우 초음파내시경을 추적관찰 함으로써 본 증례에서처럼 악성종양의 진단에 도움이 될 수 있다.
따라서 급성 특발성 췌장염에서 처음부터 악성종양을 의심하지 않을 경우에는 본 증례에서와 같은 악성종양의 진단이 늦어질 수 있다. 그러나 최근 악성종양이 의심되어 수술을 받은 후에 양성질환으로 진단되는 경우들이 보고되고 있어 수술 전 정확한 진단의 필요성이 강조되고 있으며, 이를 위해 초음파내시경을 통한 보다 정확한 진단을 위한 검사의 중요성도 증가하고 있다. 그럼에도 불구하고 전산화단층촬영, 자기공명영상, 초음파내시경으로도 원인이 밝혀지지 않은 급성 특발성 췌장염에서 악성종양을 의심하고 추적관찰하여 적절한 시기에 췌장의 악성종양을 진단하고 치료해 낸 실제 사례를 제시함으로써, 원인이 불명확한 췌장염에서 악성종양을 항상 염두에 두어야 한다는 것과 추적관찰 중 초음파내시경 사용에 대한 장점을 강조하는 측면에서 본 증례가 의의를 가진다.
Notes
Conflict of Interest
The author has no conflict to disclose.