췌관선암종이 동시에 동반된 췌장의 장액낭선종양 1예
A Serous Cystic Neoplasm of the Pancreas with Synchronous Pancreatic Ductal Adenocarcinoma
Article information
Abstract
장액낭성종양(serous cystic neoplasm)은 1978년 Compagno와 Oertel에 의해 처음으로 분류되었으며, 췌장낭성종양(pancreatic cystic neoplasm) 중 10-16%의 빈도를 나타낸다. 장액낭성종양은 악성화의 위험성이 있는 점액낭성종양(mucinous cystic neoplasm)이나 췌관내유두상점액종양(intraductal papillary mucinous neoplasm, IPMN)과는 달리 악성화의 위험성이 거의 없다고 알려져 있다. 또한 장액낭성종양은 일반적으로 고립 병터로 발견되며 췌장의 다른 낭성종양, 만성 췌장염, 췌장암과 같은 췌장 병변과 같이 존재하는 경우는 매우 드물다. 그중에서도 췌관선암종(pancreatic ductal adenocarcinoma)이 동반되는 경우는 거의 없다고 알려져 있다. 이에 저자들은 고이형성 췌장상피내종양(pancreatic intraepithelial neoplasm, PanIN)이 동반된 장액낭성종양과 인접한 위치에 췌관선암종이 동시에 발견된 증례를 문헌고찰과 함께 보고하고자 한다.
Trans Abstract
Serous cystic neoplasm (SCN) represents 10–16% of cystic pancreatic lesions, first classified by Compagno and Oertel at 1978. In contrast to mucinous cystic neoplasm or intraductal papillary mucinous neoplasm of pancreas which have malignant potential, SCN is thought to be exclusively benign as solitary lesion in nearly all cases. There has been rare reported association between the SCN and pancreatic ductal adenocarcinoma, and few cases were documented their coexistence. In this report, we present the case of SCN of the pancreas with literature review in which synchronous pancreatic ductal adenocarcinoma and pancreatic intraepithelial neoplasm coexist together.
서 론
췌장낭성종양은 1978년 Compagno와 Oertel [1]에 의해 처음 장액낭성종양과 점액낭성종양으로 분류되었다. 그중 장액낭성종양은 췌장낭성종양의 10-16%를 차지하며 악성화의 위험성이 있는 점액낭성종양이나 췌관내유두상점액종양과는 달리 악성화의 위험성이 거의 없다. 하지만 3%의 빈도로 장액낭선암종(serous cystadenocarcinoma)이 발생할 수 있기 때문에 증상이 있거나 진단이 불명확하거나 혹은 빠르게 커지는 장액낭성종양은 수술적 절제가 필요할 수 있다[1-3]. 장액낭성종양은 일반적으로 고립병터로 발견되며, 췌장의 다른 낭성종양이나 만성 췌장염과 같은 췌장 병변과 같이 존재하는 경우는 매우 드물다. 그중에서도 췌관선암종이 동반되는 경우는 거의 없다고 알려져 있다[4,5].
췌관선암종은 보통 직경이 5 mm 미만의 췌관에 발생하는 췌장상피내종양을 통해 악성화 된다. 췌장상피내종양은 분자학적인 돌연변이의 단계적 변형모델에 의해 저이형성에서 고이형성까지 진행하여 췌관선암종으로 악성화 되며 K-ras, p53, c-erbB-2 그리고 DPC4 (deleted in pancreatic cancer, locus 4)와 같은 종양성장인자들이 관여하는 것으로 생각된다[6]. 저이형성 췌장상피내종양은 정상 성인의 췌장에서도 약 40% 정도의 유병률이 있는 반면, 고이형성 췌장상피내종양은 5% 이내로 드물게 보고된다[7].
수술적 절제를 하지 않은 췌장낭성종양을 가진 환자를 추적 관찰하였을 때 진단 이후 평균 3.8 년에 췌장암이 일반 인구에 비해 22배나 높은 비율로 관찰되었으며, 특히 췌관선암종의 경우에는 낭종 자체의 악성화보다는 낭종의 근위 또는 원위부에서 새로운 종양으로 발견되었다[8]. 이렇게 서로 다른 부위에서 발생한 췌관선암종과 췌장낭성종양의 관계는 아직까지 명확하게 밝혀지지 않고 있다[9]. 다만 췌관선암종이 있는 경우 췌액에서 50%의 비율로 K-ras 돌연변이가 확인되었으며, 췌관내유두상점액종양이나 저류낭(retention cyst) 또는 점액낭성종양에서도 각각 약 60% 및 43%의 높은 비율로 K-ras 돌연변이가 발견되어 일부 췌장낭성종양의 경우에 유전학적인 변형이 인접한 위치에서 췌관선암종의 발생에 영향을 줄 수 있을 것으로 추측하고 있다[10]. 하지만 현재의 영상학적인 기법으로는 유전자 돌연변이의 특징을 조기에 관찰할 수 없으며, 장액낭성종양의 경우에는 전구세포가 중심선방세포(centroacinar cell) 표현형으로써 췌관세포에서 유래되는 다른 췌장낭성종양과는 다르며 폰 히펠 린다우(Von-Hippel-Lindau) 유전자의 돌연변이와는 연관성이 있고 K-ras나 p53의 변이가 없어 췌관선암종과의 연관성은 없다고 여겨진다. 장액낭성종양은 약 3%의 빈도로 장액낭선암종으로 악성화 되지만 조직학적으로는 장액낭성종양과 잘 구분이 되지 않는다. 다만 췌장과 췌장 주변 조직을 벗어나 원격 전이를 일으키거나, 림프혈관 또는 신경 주위를 침범하는 경우 장액낭선암종으로 진단할 수 있다[2]. 장액낭선암종은 췌관선암종과 전구세포가 달라 서로 기원이 다른 암종으로 구분될 수 있다 . 그래서 아직까지 장액낭성종양과 췌관선암종이 동시에 발견된다면 서로의 관계는 알기 어려우며, 우연적으로 동시에 발견되는 것으로 여겨진다[11]. 또한 장액낭성종양과 고이형성 췌장상피내종양이 동시에 동반된 최근의 보고에서도 두 종물의 관계를 명확히 밝혀내지 못하였다[12]. 본고에서는 고이형성 췌장상피내종양이 동반된 장액낭성종양과 인접한 위치에 췌관선암종이 동시에 발견된 증례를 문헌고찰과 함께 보고한다.
증 례
평소 건강하던 70세 남자가 내원 2개월 전 건강검진 목적으로 시행한 복부 전산화단층촬영(computed tomography, CT) 상, 췌장 미부에 50 mm 크기의 췌장 종물이 발견되어 내원하였다. 환자는 특별한 증상이 없었으며, 암을 포함한 특별한 가족력과 수술력은 없었다. 1주일에 맥주 1병 정도 마시는 음주력을 가지고 있었으며 흡연은 하지 않았다. 복부 진찰 상 장음은 감소되거나 증가되지 않았으며, 특별히 촉지되는 종괴나 압통은 없었다. 혈액 검사 상 백혈구 6,000/mm3, 혈색소 14.1 g/dL, 헤마토크릿 42.4%, 혈소판 228,000/mm3였으며 간기능 검사, 아밀라아제, 리파아제 검사는 모두 정상 소견이었다. 종양 표지자인 carcinoembryonic antigen은 2.8 ng/mL로 정상범위(0-5 ng/mL) 이내였지만, CA 19-9는 62.9 U/mL (정상범위: 0-37 U/mL)로 상승 소견을 보였다. 외부에서 시행한 복부 CT 상 췌장 미부에 50 mm의 크기를 지닌 다중격벽 구조의 분엽상 낭성종괴가 관찰되었으며, 각 낭종들은 원형모양으로 내부에 벽성결절은 없었다. 자기공명담췌관조영술(magnetic resonance cholangiopancreatography)에서는 T1-강조(T1-weighted) 상 저강도(low signal intensity), T2-강조(T2-weighted) 상 고강도(high signal intensity)의 균질한 신호가 보였으며 주췌관의 확장은 관찰되지 않아 장액낭성종양, 그중에서도 장액성과소낭선종(serous oligocystic adenoma)에 가까운 소견이었다(Fig. 1). 낭종의 크기가 크지만 영상학적으로 장액낭성종양이 의심되어 외래에서 주의 깊게 추적 관찰을 하기로 하였다.

Computed tomography (CT) and Magnetic resonance imaging (MRI) findings. (A) Axial CT scan shows lobulated cystic mass at the tail of the pancreas in an asymptomatic 70-year-old man. 50 mm sized mass has many internal locules and subtle enhancing septa. (B and C) Axial MR scans show well-defined cysts with homogenously low signal intensity on T1-weighted and high signal intensity on T2-weighted image. (D) CT scan after two months later with increased size up to 65 mm. (E and F) CT images of the cyst which has wall thickening with low attenuation mass like lesion (white arrow) adjacent to the cyst.
2개월 후 시행한 복부 CT 상에서 이전 50 mm의 크기를 지닌 다중격벽 구조의 분엽 상 낭성종괴가 65 mm로 크기가 증가하였으며, 가장 큰 분엽의 낭종 내측 부분에 낭종벽의 비대 소견과 이와 인접한 췌장 실질에 저음영의 종괴가 새롭게 관찰되었다(Fig. 1). 이상의 소견은 악성화의 가능성이 높아 환자를 설득하여 복강경을 통한 원위췌장절제술 및 비장절제술을 시행하였다. 절제된 조직의 육안 소견에서 6.5 × 4.5 × 2.5 cm 크기의 분엽 상 낭성종괴가 관찰되었고 가장 큰 분엽의 낭종 내측 부분에는 복부 CT에서 저음영으로 보였던 10 mm 크기의 또 다른 종괴가 있었으며, 벌집모양(honeycomb)의 미세낭(microcyst)들로 둘러싸여 있었다(Fig. 2). 저음영의 종괴는 고배율에서 중등도의 분화도를 보이는 선암종의 소견을 보였으며, 종괴는 췌장 주위 연조직까지 침범하였지만 대장 장간막이나 복강축 및 상장간동맥의 침범 및 림프절 전이는 없어 pT1N0M0의 췌관선암종으로 진단하였다(Fig. 3D). 저음영 주변부의 벌집모양 미세낭들은 고배율로 관찰 시 입방상피세포(cuboidal epithelium)로 둘러싸여 있어 장액낭성종양에 합당한 소견이었고(Fig. 3B), 췌관선암종과 인접해 있었다(Fig. 3A). 또한 그 주변으로 PanIN-3이 다수 발견되었다(Fig. 3C). 수술 이후 환자는 급성 합병증 없이 퇴원하였다.

Gross specimen after distal pancreatectomy with splenectomy shows that about 10 mm sized white mass-like lesion (black arrow) surrounded by the microcysts with honeycomb appearance.
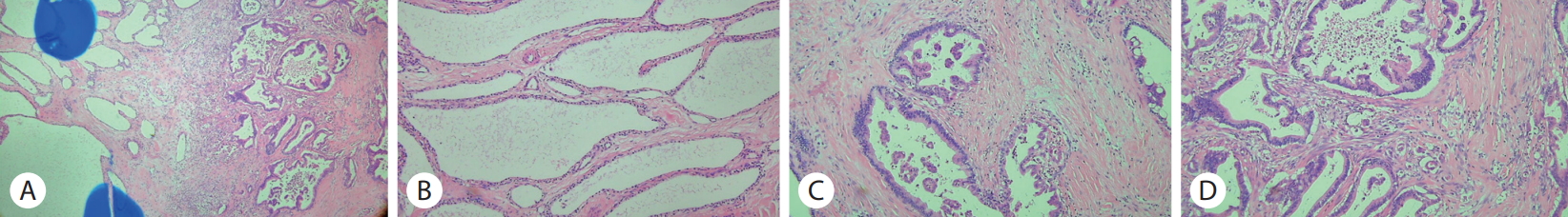
Microscopic findings. (A) Mixed lesions of cysts and adenocarcinoma (H&E stain, ×40). (B) A cystic lesion lined with a non-atypical cuboidal or flat epithelium with clear cytoplasm (H&E stain, ×200). (C) Ducts containing pancreatic intraepithelial neoplasm-3 lesions characterized by complete loss of polarity, budding of cells into the duct lumen, and significant nuclear atypia (H&E stain, ×200). (D) Adenocarcinoma lesions characterized by nuclear size variations, incomplete ductal lumens, and disorganized duct distributions (H&E stain, ×200).
고 찰
췌장암은 5년 생존율이 5% 미만으로 10 mm 이하의 작은 침윤암이라고 할지라도 수술 후 생존율이 낮아 치명적인 질환 중 하나이다. 그래서 췌장상피내종양, 점액낭성종양이나 췌관내유두상점액종양과 같은 췌장암의 전암 병변에 대한 연구가 활발히 진행 중이며, 이러한 초기 병변의 빠른 진단과 치료는 췌장암의 완치라는 측면에서 큰 기대를 받고 있다[13]. 이에 반하여 췌장낭성종양 중 10-16%를 차지하는 장액낭성종양은 현재까지 악성화의 가능성이 거의 없다고 알려져 있다. 하지만 보고에 따르면 3%의 빈도로 원격 전이를 일으키거나, 림프혈관 또는 신경 주위 침범을 하는 경우, 장액낭선암종으로 악성화가 가능하기 때문에 진단이 명확하지 않거나, 증상이 있거나, 크기가 커서 자라는 속도가 빠르다면 수술적 절제를 권고한다[2]. 췌관선암종이 단계적으로 췌관상피세포의 이형성과정으로 발생하는 것과는 다르게 장액낭선암종을 구성하는 세포들은 많은 경우 장액낭성종양과 조직학적으로 다르지 않으며, 공통적으로 과립상 세포질을 지니는 입방상피세포가 단일층의 형태로 낭을 둘러쌓고 있다. 악성이지만 림프혈관 또는 신경 주위 침범이나 췌장 주변 조직 침윤을 하는 경우가 47% 정도로 낮게 보고되었으며, 38%에서는 조직학적으로 악성과 양성을 구분할 수 없어 원격 전이를 통해서만 장액낭선암종을 진단하기도 한다[3]. 전구세포가 중심선방세포로서 점액낭성종양이나 췌관유두상점액종양과 다르기 때문에 악성화 과정도 다를 것으로 여겨진다.
췌장상피내종양은 대부분 5 mm 미만의 미세한 췌관 내에 발생하며 대부분 원주 모양의 점액 분비세포가 미세 유두나 평편한 모양으로 관내로 자라나는 형태를 보인다. 췌관내유두상점액종양과는 달리 현미경적인 병터로서 육안으로 보이지 않아 영상학적인 검사에서는 관찰되지 않고, 수술 후 우연히 발견되는 경우가 많다. KRAS2, TP53/p53, CKDN2A/P16 그리고 MADH4/CMAD4/DPC4 유전자의 단계적인 돌연변이에 의해 PanIN-1에서 PanIN-3까지 변화하며 고이형성일수록 더 많은 유전학적인 변화가 동반된다. 췌장암이 없는 성인 췌장에서 PanIN-1과 PanIN-3은 각각 40%와 5% 미만의 비율로 발견된다고 알려져 있지만, 췌장암이 있는 경우에는 PanIN-3이 30-40%까지 발견되며 높은 단계의 이형성일수록 췌장암으로 발전될 확률이 높아진다[7]. 나이가 들수록 췌장상피내종양의 유병률은 통계학적으로 유의하게 높아지며, 췌장낭성종양을 포함한 종양성 종괴가 있는 경우에도 췌장상피내종양이 동시에 동반될 가능성이 있다[6]. 췌장낭성종양을 추적 관찰하였을 때 췌장암이 일반 인구에 비해 22배나 높은 비율로 관찰되었으며, 특히 췌관선암종의 경우에는 낭종 자체의 악성화보다는 낭종의 근위 또는 원위부에서 새롭게 발견되는 경우가 있다[8]. 이렇게 서로 다른 부위에서 발생한 췌관선암종과 췌장낭성종양과의 관계는 아직까지 명확하게 밝혀지지 않고 있다[9]. 다만 K-ras 돌연변이를 동반한 췌장상피내종양의 이형성과정이 중요한 역할을 하는 것으로 추정하였다[8]. 하지만 췌장낭성종양 중에 악성화의 빈도가 낮은 장액낭성종양의 경우에는 전구세포가 다른 췌장낭성종양과는 달라 장액낭성종양에서 췌장상피내종양의 변이로 발생하는 췌관선암종이 동시에 발생되는 빈도나 기전에 대한 연구는 없다[11].
본 증례에서는 증상은 없으나 영상 검사에서 50 mm 크기의 장액낭성종양을 발견하였고 2개월 만에 크기가 65 mm로 증가하였으며, 동시에 낭종의 근위부에 고형종괴가 새롭게 발견되어 수술적으로 절제하였다. 인접한 부위에서 췌관선암종과 장액낭성종양이 동시에 진단되었으며, 그 주변으로 고이형성의 췌장상피내종양이 다수 발견된 극히 드문 사례였다. 세엽세포암종(acinar cell carcinoma) 또는 갈색세포종 (pheochromocytoma)이 췌장낭성종양과 동시에 발견된 증례가 있었지만 해당 연구에서는 낭종의 특성을 구분하지 않아 장액낭성종양이 해당 종양과 관련이 있었는지는 알기 어려웠다[14]. 또한 장액낭성종양과 고이형성 췌장상피내종양이 동시에 동반된 아주 드문 최근 증례에서도 두 종물의 관련성을 명확하게 찾을 수 없었으며, 우연히 발견되었을 가능성으로 보고하였다[12]. 본 증례에서도 장액낭성종양이 발견되었고, 비교적 짧은 기간 내에 인접한 위치에서 췌관선암종이 새롭게 관찰되었으며, 두 종양은 조직학적으로 이행구간(transition) 없이 뚜렷하게 구별되어 있었다. 췌관선암종은 췌관세포에서 기인하는 췌장상피내종양의 악성화 과정으로 발생하는 반면 장액낭성종양은 중심선방세포에서 유래된다. 이렇게 전구세포가 다르기 때문에 두 종물이 동시에 발견되는 경우는 매우 희박하다[4,5]. 그러므로 본 증례에서 발견된 췌관선암종은 장액낭성종양과는 다른 기원으로 생각해야 할 것으로 판단한다. 다만 중심선방세포와 췌관세포가 공통적으로 앞창자 유래(embryonic foregut)의 외번(outpouching)으로 발생한 구조이므로 비정상적인 외분비췌장(exocrine pancreas)의 경우에는 두 종양이 같이 존재할 수도 있다는 보고가 있다[4]. 이에 장액낭성종양과 관련이 있다고 알려진 폰 히펠 린다우 유전자의 생식세포변이나 체세포변이 또는 메틸화 중합효소 연쇄반응을 이용한 여러 유전자 연구를 통해 장액낭성종양의 유전학적인 특성을 명확히 파악하는 것이 향후 도움이 될 것으로 사료된다.
췌장암의 전 암 병변인 점액낭성종양이나 췌관내유두상점액종양은 악성화의 가능성이 있어 정기적인 추적 관찰이 필요하지만, 장액낭성종양의 경우에는 악성화 가능성이 희박하여 추적 관찰의 중요성이 상대적으로 떨어진다. 그러나 본 증례와 같이 장액낭성종양의 경우에도 기원이 다른 고이형성의 췌장상피내종양과 췌관선암종이 독립적으로 동반될 수 있어 정기적인 추적 관찰이 요구될 수 있다. 또한 추후 장액낭성종양의 악성화 과정에 대한 추가적인 연구가 필요할 것으로 사료된다.
