요약외상으로 인한 혈액담즙증은 드물지 않게 보고되고 있고 경피경간 경로를 이용한 담도내시경이나 배액술 등에 의한 의인성 손상이 증가하고 있다. 그러나 담도스텐트 제거에 따른 대량의 혈액담즙증의 보고는 매우 드물다. 본 증례는 복부 외상으로 간엽절제술을 받은 환자에서 발생한 담즙 누출을 치료하기 위해 삽입한 담도 스텐트를 제거하면서 혈액담즙증이 대량 출혈로 악화된 사례이다. 간외상 수술 후 담즙 누출로 플라스틱 담도 스텐트 삽입 후 호전 중에 혈액담즙증 및 담도염 발생으로 스텐트 교체 목적으로 제거하였으나 제거하자마자 대량의 활동성 혈액담즙증으로 악화되었다. 수술 후의 담즙 누출로 인한 주변조직 손상 및 삽입된 담도 스텐트로 인한 자극과 제거시의 손상이 원인이 될 수 있을 것으로 생각된다. 치료는 대량 출혈로 내시경 시야가 확보되지 않아 응급 혈관조영술로 지혈술을 시행하였다. 따라서 복부 외상 환자나 수술 환자에서 담즙 누출 후 담도 배액 스텐트는 일반적으로 시행되는 효과적인 치료 방법이나 혈액담즙증 및 합병증으로 담도 스텐트를 교체할 때 주변 담도나 혈관계의 합병증 유무에 대한 사전 검사를 시행하고 스텐트 제거시에도 주의를 요한다.
AbstractBiliary plastic stent induced life-threatening hemobilia is very rare. In this case, hemobilia seriously worsened following removal of a biliary stent, which had been placed for treatment of a postoperative bile leak in a patient who had undergone lateral liver segmentectomy for abdominal trauma. Following placement of the biliary stent, the bile leak improved, but hemobilia and cholangitis developed five days later. To manage the stent malfunction, we removed the biliary stent. However, life-threatening hemobilia developed immediately after removal. Endoscopic hemostasis was impossible; therefore, emergency angiographic embolization and stent graft were performed successfully. In such cases, angiographic embolization and stentgraft placement are effective diagnostic and therapeutic alternatives. When a patient develops hemobilia or cholangitis after biliary stent placement, endoscopists should pay special attention to remove the stent, which might exacerbate hemobilia.
서 론혈액담즙증(hemobilia)은 1948년 Sandblom [1]에 의해 처음 기술되었는데 간내 혈관과 담관 사이의 연결로 인해 담관으로 출혈을 일으키는 것으로 상부위장관 출혈의 드문 형태이다. 혈액담즙증의 원인은 외상, 의인성 손상, 담석, 담관염, 혈관 기형, 종양 등으로 다양한데 외상과 의인성 손상이 주요 원인이다. 또한 매우 드물지만 담도 배액 목적으로 삽입하는 플라스틱 혹은 금속 스텐트에 의한 혈액담즙증도 발생 가능하다[2,3]. 내시경적 담도 스텐트 삽입은 췌담도 내시경 분야에서 널리 시행되고 있는 주요 배액 시술 중 하나로 다양한 합병증이 보고되고 있으나 플라스틱 담관 스텐트 삽입과 관련된 혈액담즙증은 매우 드물며 현재까지 외국문헌에 한 증례가 보고되어 있다[2]. 임상적으로 혈액담즙증은 우상복부 통증, 황달, 상부위장관 출혈 등의 증상을 보일 수 있다[4,5].
저자들은 복부 외상으로 외과적 간절제를 시행 받은 후 생긴 담즙 누출로 담도 스텐트를 삽입 후 호전되었으나 혈액담즙증 및 담도염이 발생한 환자에서 담도 스텐트 교체 목적으로 스텐트 제거 후 급격히 악화된 대량의 혈액담즙증을 응급간혈관동맥 색전술로 치료한 1예를 경험하였기에 문헌 고찰과 함께 보고하는 바이다.
증 례52세 남자가 교통 사고 후 발생한 복통으로 본원 응급실을 방문하였다. 5년 전 진단받은 당뇨 외에 다른 질환은 없었고 가족력 및 사회력에서도 특이 소견이 없었다. 병원을 방문하였을때 급성병색을 보였으나 의식은 명료하였다. 활력징후는 혈압 100/70 mmHg, 맥박수 100회/분, 호흡수 19회/분, 체온 36.7℃였다. 신체 검사에서 복부는 딱딱하였고 압통 및 반발 압통이 모두 있었다. 말초혈액검사에서 백혈구 12,800/mm3, 혈색소 11.8 g/dL, 적혈구용적률 36.1%, 혈소판 343,000/mm3이었다. 혈청생화학검사에서 아스파테이트아미노전달효소 565 IU/L, 알라닌아미노전달효소 518 IU/L, 알칼리인산분해효소 66 U/L, 감마글루탐산탈수소효소 45 U/L, 총빌리루빈 0.3 mg/dL, 아밀라아제 98 IU/L, 리파아제 271 IU/L이었다.
복부 전산화단층촬영에서 좌측 간의 열상 및 혈복강으로 진단하고 응급으로 좌측엽 부분 간엽절제술을 시행하였다(Fig. 1). 간엽절제 후 13일에 후복강에 배액 위해 삽입하였던 경피 배액관의 배액량이 하루에 10 mL 이하로 감소하던 중 담즙 배액이 150 mL 이상으로 증가하기 시작해 내시경역행담도조영술을 시행하였다. 총 담관은 정상적으로 관찰되나 절제된 좌측 간엽 방향으로 간내 담관에서 조영제 누출이 확인되어 유두부괄약근절개술 시행 후 5 Fr, 12 cm 크기의 양쪽 돼지꼬리형 스텐트(Zimmon Biliary stent, COOK)를 삽입하였다(Fig. 2). 스텐트 삽입 후 담즙 배액량이 감소해 3일 후부터 담즙배액은 없었으며 복통, 발열 등의 임상 증상 역시 관찰되지 않았다. 그러나 스텐트 삽입 5일 후 환자는 갑작스런 발열, 우상복부 통증, 흑색변이 발생하면서 혈색소 수치가 11.5 g/dL에서 9.48 g/dL로 감소하였다. 상부위장관 출혈 의심 하에 증상 발생 당일 시행한 상부위장관내시경에서 십이지장 구부에 활동기에서 치유기까지 양상을 보이는 다수의 궤양이 발견되었으나 활동성 출혈 소견은 보이지 않아 프로톤펌프 억제제를 경구 투약하며 경과관찰 하였다. 그러나 상부위장관내시경 시행 4일 후부터 다시 발열과 우상 복부 통증 호소하면서 혈액검사에서 백혈구 19,880/mm3, 혈색소 8.8 g/dL, 총 빌리루빈 3.7 mg/dL 소견을 보였다. 혈액 담즙증 및 기존에 삽입된 담도 스텐트의 폐쇄로 인한 급성 담도염을 의심하여 내시경역행담도조영술을 시행하였다. 바터 팽대부에서 스텐트 주위로 소량의 출혈 소견이 관찰되어 혈액담즙증으로 생긴 혈괴로 인한 담도염이 합병된 것으로 판단하여 스텐트 교체 위해 담도 스텐트를 제거하였다. 그러나 스텐트를 제거하자마자 대량의 활동성 출혈이 발생하면서 수축기 혈압이 110 mmHg에서 80 mmHg로 감소하였다. 출혈의 위치를 명확히 찾을 수 없는 상태로 시야를 확보할 수 없어 내시경 지혈술을 시도할 수 없었고(Fig. 3), 수축기 혈압 70 mmHg 더욱 감소하여 응급으로 복부전산화단층촬영을 시행한 후 혈관조영술 및 색전술을 계획하였다. 복부전산화단층촬영에서 담즙 누출이 있어 스텐트 삽입했던 담도 주위로 타원형으로 조영되는 혈종 소견이 의심되었다(Fig. 4). 혈관 조영술에서 왼쪽 간동맥의 전분지에서 조영제의 혈관바깥누출 관찰되어 누출 부위 간동맥에 마이크로코일을 이용한 색전술 시행하였으며, 3.5 mm×19 mm 이식스텐트(graft stent)를 활동성 출혈 부위에 삽입하여 성공적으로 지혈하였다(Fig. 5). 이후 활력징후는 안정화 되었고 3세대 세팔로스포린계 항생제 정주하면서 보존 치료를 시행하였다. 경피배액관으로 추가적인 담즙 누출이 관찰되지 않고 혈색소 10.8 g/dL, 총 빌리루빈 1.2 mg/dL로 유지되어 색전술 시행 후 7일째 추가 합병증 없이 퇴원하였다.
고 찰혈액담즙증은 전형적 임상 삼징후로 담도 산통, 폐쇄성 황달, 상부위장관 출혈이 있을 경우 의심해 보아야 한다[4,5]. 원인은 크게 외상성과 비외상성으로 나눌 수 있는데 간의 외상성 손상이 주요 원인이다. 최근에는 간 및 담관 관련 시술에 의한 의인성 손상이 주요 원인이 되고 있다. 간생검이나 고주파절제(radiofrequency ablation) 후 각각 0-0.5%와 0.06-1% 빈도로 보고되고 있고, 경피담관조영술과 경피경간경로를 이용한 담도배액술은 좀더 높아 각각 0-4%와 2-10% 정도의 높은 빈도로 보고되고 있다[4-9]. 경피경간 배액술이나 담도내시경에서 혈액담즙증 합병증의 발생 빈도가 높은 이유는 담도와 혈관이 해부학적으로 인접해 있기 때문이다. 경피담즙배액관이 오랜 기간 유치되어 있는 경우 역시 혈액담즙증의 위험도가 증가한다[9-11]. 따라서 이와 같은 시술이나 복부 외상의 병력이 있는 환자에서 상부위장관 출혈이 발생하면 반드시 혈액담즙증을 의심해 보아야 한다. 그 밖에 비외상성으로 담관암 같은 악성종양, 담석, 담낭염, 간동맥 동맥류 등이 원인이 될 수 있고 담도에 삽입하는 금속 혹은 플라스틱 담도 스텐트에 의한 합병증 역시 발생 가능하다[4-9].
담도 스텐트와 관련된 전체적인 합병증은 약 5-10% 정도로 담도염, 췌장염, 출혈, 궤양, 천공, 담도 근위부나 원위부로 배액관의 이탈, 배액관의 기능장애, 담낭염 등 다양하게 발생할 수 있다[12]. 이중 출혈은 스텐트의 직접적인 접촉에 의한 위장관 출혈 뿐 아니라 본 증례에서처럼 담즙 누출을 치료하기 위해 삽입한 플라스틱 담도 스텐트에 의해서도 발생 가능하다. 담도 스텐트는 매우 드물지만 삽입 후 인접한 담도 주위 혈관에 손상을 주어 혈액담즙증을 유발하거나 스텐트 제거시 손상으로 발생할 수 있다고 보고된 바 있다[2,3].
본 증례는 수술 후 담즙 누출로 5 F 직경의 담도 스텐트를 삽입 후 호전 중에 담도 누출 부위와 인접한 부위에 혈관 손상이 발생한 것으로 추정된다. 수술 후 담즙 누출로 인한 손상인지 스텐트 자체에 의한 손상인지 전후 관계를 명확히 알 수는 없으나 이전의 증례보고에서 10 F 플라스틱 스텐트에 의한 혈액담즙증 보고가 있고[2] 스텐트 제거시 손상에 의한 가능성이 있어 담즙 누출로 인한 손상 가능성이 높은 상태에서 스텐트로 인한 이차적인 합병증의 가능성을 고려할 수 있겠다. 금속 스텐트 제거나 내시경역행담췌관조영술 자체로 인한 담도 손상에 의해 혈액담즙증이 생긴 경우와는 기전이 다르지만 작은 직경의 플라스틱 스텐트 제거시에도 혈액담즙증이 악화될 수 있다. 따라서 복부 외상환자에서는 외상 및 수술 후 발생 가능한 혈액담즙증에 대한 주의와 본 증례에서처럼 스텐트를 삽입 후 혈액담즙증이 의심되거나 관찰되는 경우 특히 기존에 삽입된 스텐트 제거시 출혈에 대한 세심한 주의가 요구된다.
혈액담즙증의 진단은 측시경을 이용하여 십이지장 유두부에서 출혈 소견을 확인하거나 내시경역행담관조영술로 담관 내에 피덩이 여부를 확인 할 수 있다. 일반적인 상부위장관내시경검사에서 유두부는 자세히 관찰하기 어려운 경우가 있어 초기 출혈이 미미한 경우 본 증례와 같이 조기 진단이 어려울 수 있다. 복부 전산화단층촬영이나 Tc-99 m 표지 적혈구 스캔은 출혈의 위치를 찾는데 유용한 검사방법이다. 선택적 동맥조영술은 진단 뿐 아니라 치료에 이용될 수 있다[4-6,13,14].
치료는 본 증례에서처럼 혈관조영술을 이용한 색전술이 효과적인 진단 및 치료 방법이다. 1976년 Walter 등[13]이 처음으로 성공적인 간동맥색전술을 보고하였고, 최근에는 선택적인 도관술의 발전으로 혈관조영술 및 색전술을 혈액담즙증의 초기치료로 사용하고 있다. 혈관조영술 및 색전술은 수술에 비해 덜 침습적이므로 본 증례의 환자와 같이 활력징후가 불안정한 환자들에 가장 효과적인 치료로 널리 인정되고 있다[14].
결론적으로 복부 외상 및 수술 환자에서 담즙 누출 후 담도 배액 스텐트는 일반적으로 시행되는 효과적인 치료방법이나 스텐트 삽입 후 원인 미상의 혈액담즙증에 의한 담도폐쇄 증상이 있어 스텐트 교체 등이 필요한 경우 복부전산화단층촬영 등의 사전 검사를 통한 주변 연관 구조물을 파악하고 새로운 합병증 발생 유무에 대한 확인이 필요하다. 또한 담도 스텐트를 제거할 때에도 스텐트 자체에 의한 손상이 발생할 수 있음을 주지하고 합병증이 발생할 경우 신속하고 적절한 대응이 필요하다.
REFERENCES1. Sandblom P. Hemorrhage into the biliary tract following trauma; traumatic hemobilia. Surgery 1948;24:571-586.
2. Conio M, Caroli-Bosc FX, Buckley M, et al. Massive hematobilia after extraction of plastic biliary endoprosthesis. J Clin Gastroenterol 1997;25:706.
3. Wolters F, Ryan B, Beets-Tan R, et al. Delayed massive hemobilia after biliary stenting. Endoscopy 2003;35:976-977.
4. Bloechle C, Izbicki JR, Rashed MY, et al. Hemobilia: presentation, diagnosis, and management. Am J Gastroenterol 1994;89:1537-1540.
7. Savader SJ, Trerotola SO, Merine DS, Venbrux AC, Osterman FA. Hemobilia after percutaneous transhepatic biliary drainage: treatment with transcatheter embolotherapy. J Vasc Interv Radiol 1992;3:345-352.
8. Willner IR, El-Sakr R, Werkman RF, Taylor WZ, Riely CA. A fistula from the portal vein to the bile duct: an unusual complication of transjugular intrahepatic portosystemic shunt. Am J Gastroenterol 1998;93:1952-1955.
10. Shah RJ, Adler DG, Conway JD, et al. ASGE Technology committee. Cholangiopancreatoscopy. Gastrointest Endosc 2008;68:411-421.
11. Jeng KS, Sheen IS, Yang FS. Vascular complications in percutaneous transheaptic management of complicated hepatolithiasis with difficult intrahepatic biliary stricture: are they avoidable? Surg Laparosc Endosc Percutan Tech 2002;12:82-87.
12. Raijman I. Biliary and pancreatic stents. Gastrointest Endosc Clin N Am 2003;13:561-592.
Fig. 2.The ERCP finding shows a contrast leak (yellow arrow) in the left intrahepatic bile duct (A) and a biliary stent subsequently inserted to prevent a bile leak (red arrow, B). 
Fig. 3.Duodenoscopic findings before and after removal of the biliary stent. Minor hemobilia was noted in the ampulla of Vater (A) and active bleeding in the ampulla of Vater (B) following removal of the biliary stent. 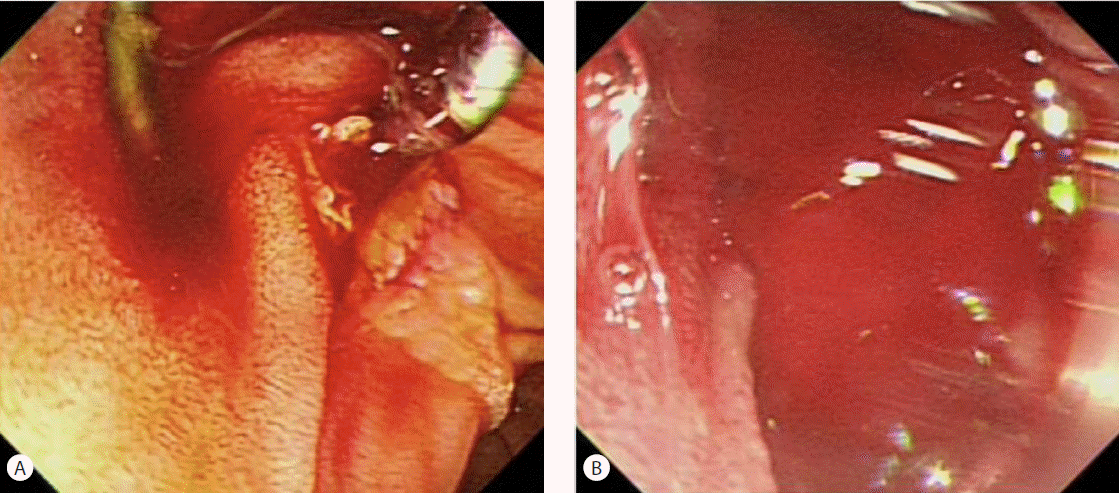
Fig. 4.Emergency follow-up abdomen CT shows an enhanced hemorrhagic cystic lesion (arrows) in the left medial side. 
Fig. 5.A hepatic artery angiogram shows active bleeding from segmental branch bifurcation of the right anterior branch of the hepatic artery (A). Therapeutic embolization was performed in the left hepatic artery using three microcoils, and a 3.5 mm × 19 mm graft stent was placed at the active bleeding focus (arrow, B). 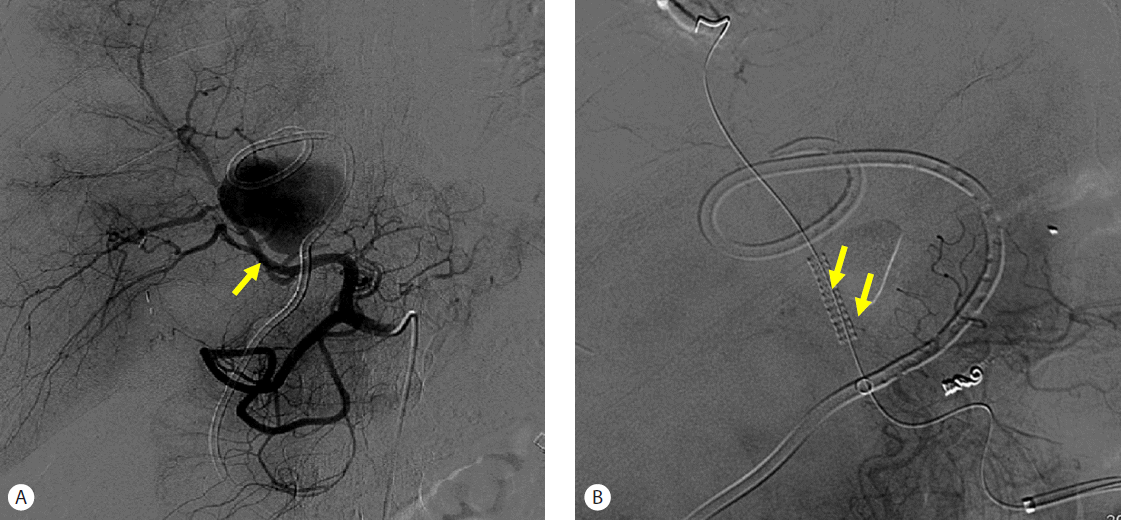
|
|
|||||||||||||||||||||||||||||||||||