선행항암화학요법 후 근치적 절제한 진행성 혼합 간세포-담관암종 1예
요약
혼합 간세포-담관암종은 조직학적 특성이 다양한 원발성 간암의 드문 형태이다. 혼합 간세포-담관암종의 근치적 치료법은 수술적 절제가 유일하나, 진행성 혼합 간세포-담관암종의 치료에 대해서는 잘 정립되어 있지 않다. 저자들은 진행성 혼합 간세포-담관암종에서 선행항암화학요법을 시행 후 근치적 수술이 가능하였고, 수술 15개월 후까지 재발을 보이지 않은 증례를 보고하는 바이다.
Keywords: 선행항암화학요법, 혼합 간세포-담관암종
Abstract
Combined hepatocellular-cholangiocarcinoma (HCC-CC) is a primary liver cancer with histopathologic features of both hepatocelluar carcinoma and cholangiocarcinoma. As combined HCC-CC has been associated with poor outcomes, accurate diagnosis and proper treatment planning for patients are considered to be important for improving survival. Currently, surgery is known as the only treatment modality offering potential cure for localized disease. However, there are little published treatment options for advanced or recurrent disease. Furthermore, no published reports exist in respect to the applying successful curative resection after neoadjuvant therapy for advanced combined HCC-CC. Here, we report a case of combined HCC-CC subtype with stem cell feature, intermediate type who underwent curative surgical resection after neoadjuvant chemotherapy consisting of cisplatin and gemcitabine. Pathologic report revealed negative resection margin and follow-up imaging study shows no evidence of tumor recurrence.
Keywords: Combined hepatocellular-cholangiocarcinoma, Neoadjuvant chemotherapy, Curative resection
서 론
혼합 간세포-담관암종(combined hepatocellular-cholangiocarcinoma, HCC-CC)은 같은 종양 내에 간세포암종과 담관암종의 특징을 동시에 가지고 있는 원발성 간암의 한 형태로서 문헌에 따라 1-14.2%로 발생률이 다양하다[ 1- 3]. 수술적 절제가 완치를 기대할 수 있는 유일한 치료법으로 알려져 있으나 절제 불가능한 진행성 혼합 간세포-담관암종의 치료는 잘 알려져 있지 않다. 경동맥화학색전술과 같은 국소치료의 효과는 전형적인 간세포암종과 달리 제한적이다. 또한 수술 후 재발 또는 전이된 혼합 간세포-담관암종에서 항암화학요법을 시행한 소수의 증례 보고들이 있으나 항암화학요법의 효과에 대해서는 불분명한 상태이다[ 4, 5]. 특히 수술 전 선행항암화학요법을 시행 후 수술적 완전 절제가 가능하였던 증례는 지금까지 보고된 바 없었다. 이에 저자들은 진행성 혼합-간세포 담관암종에서 수술 전 선행항암화학요법 시행 후 완전 절제가 가능하였고 수술 후 15개월 동안 재발 없이 추적관찰 중인 증례를 경험하였기에 보고하고자 한다.
증 례
49세 남자가 2일 전 발생한 우상복부 통증과 발열을 주소로 내원하였다. 신체검진에서 만성 간질환을 시사하는 소견은 없었다. 일반혈액검사에서 혈색소 12.9 g/dL, 백혈구 7,260/mm 3, 헤마토크리트 38.2%, 혈소판 353,000/mm 3였고, 혈청 생화학 검사에서 BUN 7 mg/dL, creatinine 0.8 mg/dL, 총 단백 6.9 g/dL, 알부민 4.4 g/dL, AST/ALT 31/22 IU/L, 총 빌리루빈 0.6 mg/dL, ALP 178 IU/L, GGT는 145 IU/L였다. B형 간염 항원 및 항체 그리고 C형 간염 항체는 음성이었다. CEA는 2.3 ng/mL, CA19-9는 18 U/mL였다. 복부 computed tomography (CT)에서 담낭 기저부에 경계가 불명확한, 조영증강이 잘 되지 않는 종괴가 주위의 간실질과 담관 분지를 침윤하였다. 문맥대정맥(portocarval) 림프절, 총간동맥(common hepatic artery) 림프절 및 대동맥 주위 림프절(para-aortic lymph node) 종대가 관찰되었다( Fig. 1A- C). 복부 magnetic resonance imaging (MRI)에서 종괴는 T1 강조영상에서 저신호 증강 및 T2 강조영상에서 고신호 증강을 보였다( Fig. 2). 양성자방출단층촬영(positron emission tomography-computerized tomography, PET-CT)에서 fluorodeoxyglucose (FDG) 섭취의 증가가 관찰되었다( Fig. 3A, B). 초음파 유도하 경피적 간생검에서 중등도의 분화도를 보이는 선암이었다. 담낭암의 간 침범, 다발성 림프절 전이로 여겨 gemcitabine (1,000 mg/mm 2)과 cisplatin (25 mg/mm 2)을 제1일과 8일에 3주 간격으로 정주하는 복합항암화학요법을 시작하였다. 항암 치료 6주기 시행 후 추적 복부 CT에서 종괴의 크기가 현저히 감소하였다( Fig. 1D). PET-CT에서 역시 종괴 및 림프절의 FDG 섭취가 현저히 감소하였다( Fig. 3C, D). 우측 간문맥색전술을 시행하여 간좌엽 용적을 늘린 후 담낭과 담관 및 주위 림프절 절제를 포함한 확대 우간절제술을 시행하였다. 육안소견에서 종양은 약 5 × 3 cm 크기의 단일 종괴였으며 담낭의 점막 부위에 간 실질과 직접적인 연속성을 보이는 황색의 결절성 병변이 내강 내로 돌출되어 있었다( Fig. 4). 현미경 소견에서 종양은 크게 두 가지 조직 형태로 구분되었다. 일부 결절을 구성하는 세포는 치밀한 육주(trabeculae) 배열을 보이는 투명세포가 세포주를 형성하고 있어 간세포암종부위였고( Fig. 5A) 이 중 종양세포 일부가 비교적 일정한 형태의 조직구와 염증 세포들로 치환되어 있어 항암효과가 있는 부분으로 여겨졌다( Fig. 5B). 다른 조직 형태는 비교적 크기가 작고 소량의 세포질을 가진 세포들이 고형소(solid nest)를 형성하고 있었다. 이들은 일부 샘 모양 구조를 보였으나 명확한 내강을 보이는 샘 형성은 없었으며 주위에 교원질 침착으로 인한 섬유화를 동반하고 있어 담관암종부위로 생각하였다( Fig. 5C). 림프절 전이는 없었다. 면역조직화학염색 결과 간세포암종과 유사하게 보였던 세포들은 glypican-3에 염색되었고( Fig. 5D), 담관암종부위는 cytokeratin (CK) 19에 부분적으로 염색되었다( Fig. 5E). 두 가지 형태의 세포는 모두 간줄기세포(stem cell) 표지자인 EpCAM에 염색되었다( Fig. 5F, G). 담낭에서 보이는 종양은 분명한 샘 형성은 없고 일부 육주 형태를 보였다. 이들은 면역조직화학염색에서 glypican-3에 양성을 보여 간세포암종의 담낭 침범으로 여겨졌다. 이들도 EpCAM에 염색되었다. 이상으로 줄기 세포 특징을 가지는 혼합 간세포-담관암종, 중간 세포 아형(combined HCC-CC with stem cell feature, intermediate cell subtype)로 진단하였다. 환자는 수술 15개월 후 시행한 추적 복부 CT에서 현재까지 재발 없이 추적 관찰 중이다.
고 찰
본 증례는 담낭암의 간침범 및 다발성 림프절전이로 오인하여 gemcitabine과 cisplatin 항암요법 후 현저히 호전되어 근치적 절제수술을 시행한 혼합 간세포-담관암종 예이다.
1903년 Wells에 의해 처음 보고된 후, 1949년 Allen과 Lisa에 의해 혼합 간세포-담관암종이라는 용어가 처음 기술되었고[ 5, 6], 이후 보고자에 따라 여러 유형으로 분류된 바 있다[ 7, 8]. 가장 최근 제시된 2010년 WHO 분류에서는 혼합 간세포-담관암종을 크게 고전형(classical type)과 줄기세포 특징을 가지는 아형으로 분류하고 줄기세포 특징을 가지는 혼합 간세포-담관암종을 세 가지 아형으로 분류하였다; a) stem cell features with typical subtype; b) stem cell features with intermediate-cell type; and c) stem cell features with cholangiocellular subtype. 본 증례는 혼합 간세포-담관암종 줄기세포 특징을 가지는 아형의 중간형에 해당된다[ 1, 3]. 이는 하나의 종양 내 간세포암종과 담관암종의 중간형태를 보이면서면역조직화학염색에서 간세포(alphafetoprotein [AFP], HepPar-1, CK8, CK18, glypican-3), 담관세포(CK7, CK19, CEA) 표지자 및 두 종양으로 분화가 가능한 간줄기세포(c-kit, EpCAM) 표지자에 동시에 양성을 보이는 경우로 본 증례와 부합한다. 혼합 간세포-담관암종은 전형적인 간세포암종이나 담관암종과 다른 임상양상 및 경과를 보이는 원발성 간암의 한 형태로, 드문 질환이나 대부분 수술 후 병리소견으로 확진된다는 점을 감안하면 실제 발생률은 보고된 것보다 높을 것으로 여겨진다. 혼합 간세포-담관암종은 종양 표지자인 AFP 상승이 흔하고, CEA 및 CA19-9는 정상인 경우가 많아 전형적인 간세포암종과의 감별이 어렵다. 또한 종양을 구성하는 두 암종의 비율 및 섬유화 정도에 따라 다양한 조직학적 특징을 보여 영상 검사의 역할도 제한적이다. 이러한 이유로임상 정보만으로 혼합 간세포-담관암종을 의심하는 것은 매우 어렵다. 저자들은 본 증례를 담낭암의 간침범 및 다발성 림프절전이로 오인하였다. 이러한 이유로 첫째, 환자가 바이러스성간염이나 간경변 등 기저 간질환 병력이 없었고, 둘째, 복부 CT와 MRI에서 조영증강 등의 영상소견이 담낭암이나 담관암 등의 선암종에 합당하여 비교적 흔하지 않은 간세포암종의 담낭침범보다는 주로 담낭에 위치한 종괴가 간침범을 하고 있다고 여겼으며, 셋째, 또한 영상소견에서 다발성 침프절 종대 소견으로 림프절 전이를 의심하였고 이는 간세포암종보다는 담관암종이나 담낭암에서 흔하며, 넷째, 수술 전 초음파 유도하 간생검에서 선암이었기 때문이다. 수술 전 간세포암종을 의심하지 않아 AFP 검사를 시행하지 않았다. 일반적인 조직 생검으로는 본 증례에서처럼 간세포암종이나 담관암종의 일부 세포만이 보일 수 있으므로 주의가 필요하다. 하지만 간 및 경부 림프절 생검만으로도 혼합 간세포-담관암종을 진단한 보고도 있어 전형적인 간세포암종 또는 담관암종의 임상경과를 보이지 않는 간종괴의 경우 혼합 간세포-담관암종의 가능성을 의심하고 적극적인 조직검사 및 면역화학염색을 통해 진단하려는 노력이 필요할 것으로 여겨진다[ 9]. 혼합 간세포-담관암종은 병기가 낮고 간기능이 양호한 경우 수술적 치료가 완치를 기대할 수 있는 유일한 치료법으로 알려져 있으나 혼합 간세포-담관암종은 문맥 침범을 잘하는 간세포암종의 특징과 림프절 전이를 잘하는 담관암종의 특징을 모두 가지고 있어 수술 후 재발률이 높다[ 10, 11]. 수술이 불가능한 진행성 혼합 간세포-담관암종의 치료에 대해서는 알려진 바가 거의 없다. 전형적인 간세포암종에서 국소치료법은 정립된 치료 방법이지만, 혼합 간세포-담관암종에서 고주파열치료는 수술적 절제보다 생존율 향상을 보여주지 못하였다. 경동맥화학색전술 역시 섬유성 간질이 풍부하고 간동맥에서 공급받는 혈류가 많지 않은 특성으로 인해 반응이 좋지 않다. 따라서 진행성 혼합 간세포-담관암종에서 항암화학요법은 중요하나, 현재까지 그 역할은 잘 알려지지 않았다. 또한 혼합 간세포-담관암종에서 선행항암화학요법(neoadjuvant chemotherapy) 후 완전한 절제를 시행한 증례는 보고된 바가 없었다. 저자들은 본 증례에서 처음부터 선행항암화학요법을 목적으로 항암 치료를 고려하지는 않았다. 진단 당시 간 침범을 동반한 담낭암으로 생각하고 다발성 림프절 전이를 의심하여 수술이 어렵다는 판단 하에 항암화학요법을 시행하였다. 본 증례는 gemcitabine과 cisplatin을 병용하여 3주 간격으로 6주기 치료한 결과 부분 반응을 보였다. 또한 진단 당시 전이를 배제할 수 없었던 복부 림프절은 추적 PET-CT에서 FDG 대사 섭취와 크기가 감소하여 염증으로 인한 이차 변화 가능성도 있다고 생각하고 수술을 시행하였다. 하지만 현재 진단법으로는 림프절 전이 여부를 명확하게 알 수 없어 본 증례의 수술 가능 여부에 대한 이견은 있을 것으로 여겨진다.
본 증례는 수술 후 병리판독에서 담관암종보다는 간세포암종을 구성하는 세포들이 주로 염증세포나 조직구로 치환되어 있어 간세포암종이 항암화학요법에 좋은 반응을 보였다고 여겨진다. 진행성 담관암종에서 gemcitabine과 cisplatin의 병용요법이 생존율 향상이 있다고 보고된 바 있고[ 12] 간세포암종은 경구용 항암 표적치료제인 sorafenib에 생존 연장 효과가 입증된 것 외에[ 13] 항암화학요법에 반응이 좋지 않은 점을 고려해 볼 때 특이하다. 본 증례는 현재 15개월 추적관찰 중으로 재발의 증거는 없으나 혼합 간세포-담관암종, 특히 줄기세포 형태는 간세포암종 또는 담관암종 단독보다 재발이나 전이가 흔하여 예후가 더 안 좋은 것으로 알려져 있어[ 14, 15] 향후로도 밀접한 추적관찰을 요한다.
REFERENCES
1. Singh S, Chakraborty S, Bonthu N, Radio S, Hussain SM, Sasson A. Combined hepatocellular cholangiocarcinoma: a case report and review of literature. Dig Dis Sci 2013;58:2114-2123.   2. Jarnagin WR, Weber S, Tickoo SK, et al. Combined hepatocellular and cholangiocarcinoma: demographic, clinical, and prognostic factors. Cancer 2002;94:2040-2046.   3. O’Connor K, Walsh JC, Schaeffer DF. Combined hepatocellular-cholangiocarcinoma (cHCC-CC): a distinct entity. Ann Hepatol 2014;13:317-322.  4. Chi M, Mikhitarian K, Shi C, Goff LW. Management of combined hepatocellular- cholangiocarcinoma: a case report and literature review. Gastrointest Cancer Res 2012;5:199-202.   6. Allen RA, Lisa JR. Combined liver cell and bile duct carcinoma. Am J Pathol 1949;25:647-655.   7. Taguchi J, Nakashima O, Tanaka M, Hisaka T, Takazawa T, Kojiro M. A clinicopathological study on combined hepatocellular and cholangiocarcinoma. J Gastroenterol Hepatol 1996;11:758-764.   8. Goodman ZD, Ishak KG, Langloss JM, Sesterhenn IA, Rabin L. Combined hepatocellular-cholangiocarcinoma. A histologic and immunohistochemical study. Cancer 1985;55:124-135.   9. Kang HW, Park JJ, Moon IH, et al. The mixed hepatocellular-cholangiocarcinoma confirmed by liver and neck node biopsy. Ewha Med J 2009;32:79-84.  10. Lee SD, Park SJ, Han SS, et al. Clinicopathological features and prognosis of combined hepatocellular carcinoma and cholangiocarcinoma after surgery. Hepatobiliary Pancreat Dis Int 2014;13:594-601.   11. Yin X, Zhang BH, Qiu SJ, et al. Combined hepatocellular carcinoma and cholangiocarcinoma: clinical features, treatment modalities, and prognosis. Ann Surgi Oncol 2012;19:2869-2876.  12. Valle J, Wasan H, Palmer DH, et al. Cisplatin plus gemcitabine versus gemcitabine for biliary tract cancer. N Engl J Med 2010;362:1273-1281.  13. Llovet JM, Ricci S, Mazzaferro V, et al. Sorafenib in advanced hepatocellular carcinoma. N Engl J Med 2008;359:378-390.  14. Zhan Q, Shen BY, Deng XX, et al. Clinical and pathological analysis of 27 patients with combined hepatocellular-cholangiocarcinoma in an Asian center. J Hepatobiliary Pancreat Sci 2012;19:361-369.   15. Lee JH, Chung GE, Yu SJ, et al. Long-term prognosis of combined hepatocellular and cholangiocarcinoma after curative resection comparison with hepatocellular carcinoma and cholangiocarcinoma. J Clin Gastroenterol 2011;45:69-75. 
Fig. 1.
Liver CT findings. (A) There is an ill-defined low attenuation mass in the liver and the gallbladder fundus. Porto-caval lymph node enlargement is shown (arrow). (B) Para-aortic lymph node enlargement is shown (arrow). (C, D) After 6 cycles of combined gemcitabine and cisplatin treatment, the mass is markedly decreased. CT, computed tomography. 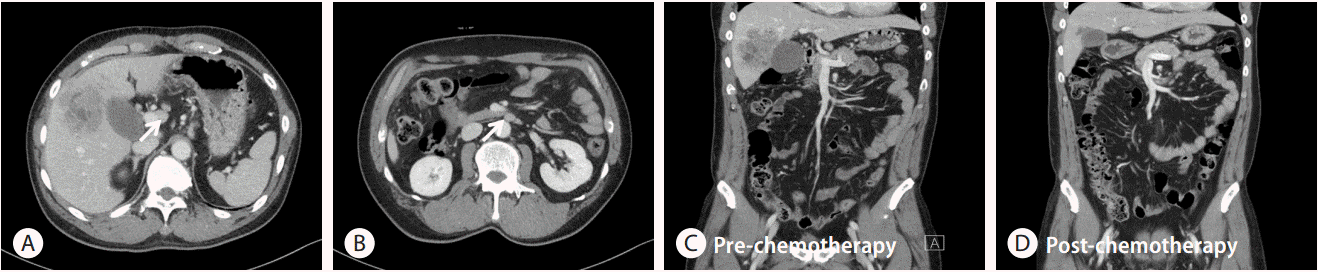
Fig. 2.
Liver MRI findings. (A) T1-weighted MR image shows an illdefined low signal intensity mass in the gallbladder fundus invading the liver and penetrating the liver capsule. (B) T2-weighted MR image shows a high signal intensity mass. MRI, magnetic resonance imaging; MR, magnetic resonance. 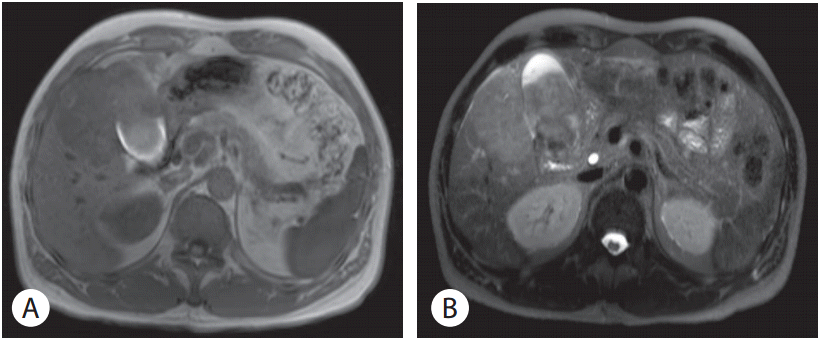
Fig. 3.
PET-CT findings. (A) There is an increased FDG uptake (SUV=12.4) mass in the liver and the gallbladder fundus. Increased FDG uptake (3.6) of porto-caval lymph node is shown (arrow). (B) Increased FDG uptake (3.5) of para-aortic lymph node is shown (arrow). (C, D) After 6 cycles of combined gemcitabine and cisplatin treatment, the mass and the lymph nodes (arrows) show decreased metabolism. PET-CT, positron emission tomographycomputerized tomography; FDG, fluorodeoxyglucose; SUV, standardized uptake value. 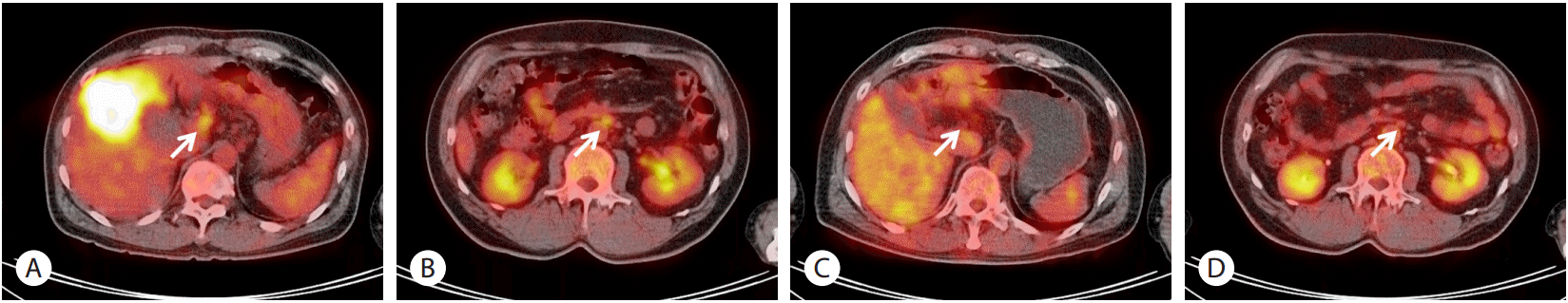
Fig. 4.
Gross finding of resected specimen. The 5 × 3 cm sized ill-defined mass is shown in the liver in continuity with the adjacent gallbladder. 
Fig. 5.
Microscopic (A-C) and Immunohistochemical findings (D-G). (A) Hepatocellular carcinoma component shows trabecular patterns composed of clear cells (H&E stain, ×100). (B) Some of hepatocellular carcinoma component is replaced by histiocytes and inflammatory cells indicative of chemotherapy responsiveness (H&E stain, ×100). (C) Cholangiocarcinoma component shows mixtures of small and round shaped tumor cells in solid nest within the fibrous stroma (H&E stain, ×100). (D) Hepatocellular carcinoma component is immunoreactive for glypican-3 but histiocytes and inflammatory cells (arrows) are not stained (×40). (E) Cholangiocarcinoma component is partially immunoreactive for Cytokeratin 19 (×40). (F, G) Both hepatocellular and cholangiocarcinoma components immunoreactive for EpCAM (×100). 
|
|

















