서 론
신경내분비종양 환자를 대상으로 소마토스타틴 수용체 표적 펩티드에 방사성동위원소를 표지하여 시행하는 핵의학 치료는 유럽, 호주 등지에서 10여 년 전부터 시행되었다. 옥트레오스캔(octreoscan) 또는 Ga-68 DOTATOC positron emission tomography (PET) 등 소마토스타틴 수용체 표적 기능 영상은 소마토스타틴 발현을 치료 전에 확인함으로써 효과가 있을 환자를 사전 선별할 수 있고 표적능이 뛰어나 다른 항암치료에 비해 부작용이 적고 치료 효과가 좋다. 그러나 DOTATOC, DOTATATE 등 표적 물질이 특허가 없고 신경내분비종양이 희귀하여 제약회사의 관심이 없어 임상시험이 이루어지지 않아 신약허가를 받지 못하여 동정적 치료가 가능한 일부 국가에서만 시행되었다. 우리나라는 한동안 환자를 독일, 말레이시아 등 외국으로 보내 치료를 하였다. 프랑스의 Advanced Accelerator Applications (AAA) 회사에서 Lu-177 DOTATATE 치료제(Lutathera®)로 다국적 임상시험을 하였고 유럽, 미국에서 신약으로 등재되었다. 우리나라에서는 저자와 신경내분비 종양 환우회의 노력으로 2019년 10월 한국희귀·필수의약품센터를 통해 치료를 시작하였고 2020년 7월 식품의약품안전처에서 품목허가를 하였다. 이제 기능적 핵의학 진단과 치료가 국내에서 가능해져 리뷰를 하고자 한다.
본 론
1. 기능 영상
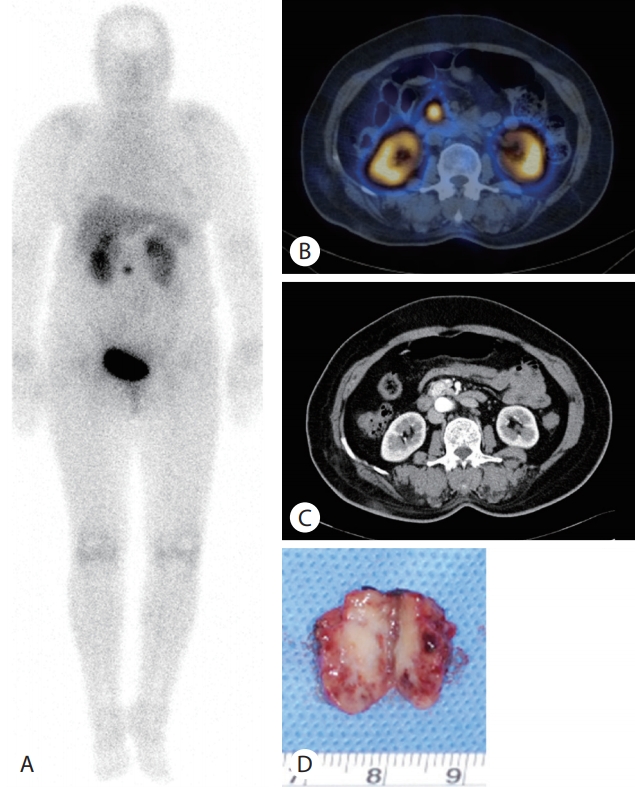
췌장 등에서 발생하는 신경내분비종양은 인슐린종, 글루카곤종, 가스트린종 등 기능성이든 비기능성이든 관계없이 대부분 소마토스타틴 수용체를 발현한다. 내인성 소마토스타틴은 혈중에서 안정적이지 않기 때문에 여러 종류의 소마토스타틴 억제제들이 개발되었는데, 옥트레오타이드(octreotide), 란레오타이드(lanreotide) 등이 있다. 소마토스타틴과 구조가 유사한 합성단백약물인 옥트레오타이드에 방사성동위원소를 표지하여 환자에 주사하면 신경내분비종양에 선택적으로 섭취되어 기능적 핵의학영상이 가능하다. 대표적인 예로 111In-옥트레오타이드를 이용한 옥트레오스캔이 있는데 감마카메라를 이용한 전신스캔으로 진단한다(Fig. 1). 이전 연구 결과를 살펴보면 옥트레오스캔은 computed tomography (CT), magnetic resonance imaging (MRI)보다 우수하여 48명 환자의 83개 병변 중 72개(87%)를 찾은 반면 CT는 33개(44%), MRI는 29개(43%)를 찾았다[1]. Single photon emission computed tomography (SPECT)/CT를 이용하면 더욱 정확한 진단을 할 수 있다. 49명의 환자에서 스캔, SPECT, SPECT/CT를 비교한 연구를 보면 SPECT/CT가 89개의 섭취 부위 중 25개(28%)의 병변을 더욱 정확히 분별할 수 있어 추가적인 병소를 찾거나 염증을 구별하고 생리학적 정상 섭취를 구별할 수 있었다[2].
최근 옥트레오타이드 유사체를 이용한 PET용 방사성 의약품이 개발되었다. 양전자를 방출하는 Ga-68을 표지한 DOTATOC, DOTATATE, DOTANOC인데 이 중 국내에서는 Ga-68 DOTATOC PET/CT가 가능하다. Ga-68 DOTATOC PET/CT를 In-111 옥트레오타이드 SPECT와 비교한 전향적 연구에 의하면 27명의 신경내분비종양 환자에서 PET/CT는 279개의 병변을 찾았으나 SPECT는 157개의 병변을 찾았다[3]. 이는 PET/CT가 SPECT에 비해 해상도가 좋기 때문이다. 소마토스타틴 유도체 PET/CT의 신경내분비종양 진단능 평가를 위해 Ga-68 표지 소마토스타틴 수용체 PET/CT 연구 21개와 Cu-64 표지 소마토스타틴 수용체 PET/CT 연구 1개, 총 2,105명의 환자를 대상으로 한 메타분석에 따르면 소마토스타틴 유도체 PET/CT의 신경내분비종양 진단 예민도는 93% (95% 신뢰구간 91-94%), 특이도는 96% (95% 신뢰구간 95-98%)로 평가되었다[4].
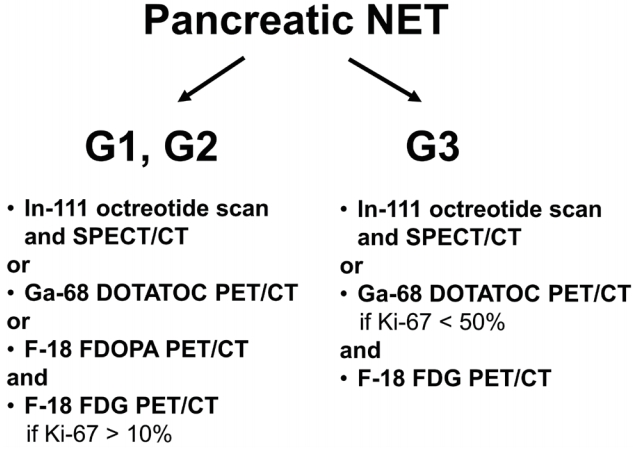
G1, G2와 같이 잘 분화된 신경내분비 종양에서는 F-18 fluorodeoxyglucose (FDG) PET 영상에서 섭취가 거의 없는데 비해, G3와 같이 분화도가 나쁜 경우 소마토스타틴 표적 기능 영상에서는 잘 보이지 않고 FDG PET에서 잘 보인다. 28명을 대상으로 한 연구에서 분화도가 좋아도 FDG 섭취가 높을 경우 무진행생존기간 및 총생존기간이 짧았다[5]. G3의 경우에도 분화도가 좋으면 소마토스타틴 표적 기능 영상에서는 잘 보이는 경우가 있다(Fig. 2).
Ga-68은 물리적 반감기가 68분인 양전자방출 핵종으로, 반감기가 271일인 Ge-89/Ga-68 발생기를 이용하여 생산이 가능하다. 따라서 F-18과 달리 사이클로트론이 없어도 PET 검사를 할 수 있으나 발생기 가격이 수천만 원에 이르러 일부 병원에서만 사용하고 있고 상업적 대량 생산이 어려워 Ga-68 DOTATOC을 구입할 수 없어 PET/CT가 있어도 검사를 못하는 병원이 많다.
소마토스타틴 수용체 기능 영상은 다음과 같은 목적으로 사용될 수 있다[6].
• 작은 기능성 종양의 원발 병소 위치를 찾거나 선암과 감별진단
• 병기 판정
• 치료 후 효과 판정 및 재발 병소 진단
• 옥트레오티드 치료에 적응이 될 환자 선별
• 소마토스타틴 수용체 방사성핵종 치료 대상 환자 선별
신경내분비종양은 세포들의 아민 전구물질 섭취 및 탈카르복실화라는 대사과정과 밀접한 관련이 있기 때문에 APUDoma라 불릴 정도로 아민 대사와 밀접한 연관을 가지고 있다. 아민 전구물질로 L-DOPA는 세포 내에서 도파민과 세로토닌으로 변환되며 세포질 내의 분비과립에 저장되고, 자극에 의해 세포 밖으로 배출된다. 이러한 성질을 이용하여 F-18 FDOPA가 신경내분비 종양의 PET 영상에 이용된다. F-18 FDOPA PET/CT는 65-85%의 예민도로 Ga-68 DOTATOC PET/CT에 비해 낮으나 Ga-68이 없는 경우 대신할 수 있는 검사이다.
2. 펩타이드 수용체 방사성핵종 치료(peptide receptor radionuclide therapy, PRRT)
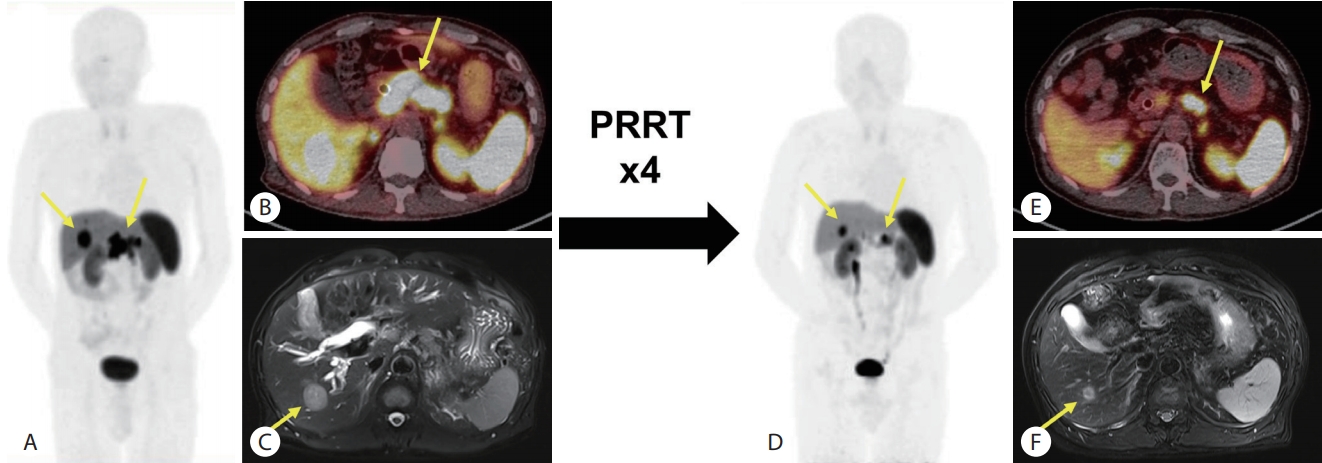
표적 영상진단에 사용되는 바이오마커는 같은 원리로 표적치료도 가능한데 베타선을 내는 방사성핵종을 표지한 Y-90 DOTATATE나 Lu-177 DOTATATE를 이용한 PRRT로 전이성 신경내분비종양을 치료할 수 있다(Fig. 3). Lu-177은 베타선과 감마선을 동시에 방출하여 고용량의 Lu-177 DOTATOC을 이용하면 치료뿐만 아니라 전신스캔 및 SPECT/CT를 촬영하여 섭취 정도를 모니터링을 할 수 있다.
허가 받지 않은 의약품을 다른 치료 방법이 없는 경우 동정적 치료를 할 수 있는 독일, 호주 등에서는 신경내분비종양 치료로 PRRT를 20년 이상 사용하였으나 특허가 만료되고 희귀 질환이어서 어느 제약회사도 허가를 위한 임상시험을 하지 않았다. 프랑스의 AAA라는 제약회사가 이미 임상적 사용 경험이 많고 미국 Food and Drug Administration에서 희귀의약품으로 지정 받아 임상시험을 하고 품목허가를 받으면 7년간의 독점권을 받는 것에 착안하여 중간창자 신경내분비종양 환자를 대상으로 Lu-177 DOTATATE 치료에 대한 다기관 3상 임상시험인 NETTER-1을 수행하였다. 치료군 116명의 환자에서 7.4 GBq의 Lu-177 DOTATATE를 8주 간격으로 4회 투여하고 대조군 113명의 환자에게는 60 mg의 장반감기 옥트레오타이드를 4주 간격으로 투여하여 비교한 결과 20개월 추적 무진행 생존율이 치료군은 65.2%, 대조군은 10.8%로 유의하게 치료군이 높았다[7]. 치료군의 G3-4 호중구 감소, 혈소판 감소, 림프구 감소는 각각 1%, 2%, 9%였으며 관찰 기간 중 신장독성은 나타나지 않았다. 이 임상시험의 결과를 근거로 Lu-177 DOTATATE (Lutathera®)는 유럽, 미국에서 각각 2017년, 2018년 위장관췌장 신경내분비종양 환자를 치료할 수 있는 신약으로 등재되었다[8]. 핵의학치료 신약의 상품가치를 인정받아 AAA사는 39억 달러에 노바티스로 인수되었다.
우리나라에서는 신경내분비종양 환자들이 해외원정 치료를 받아왔고 2019년 10월부터 한국희귀·필수의약품센터를 통해 개인이 구매하여 서울대학교병원, 서울아산병원 등 핵의학과에서 치료를 시작하였다. 저자와 신경내분비종양 환우회는 노바티스와 협의하여 식품의 약품안전처에 신약허가를 위한 신청을 하였고 신속심사를 통해 2020년 7월 품목허가를 받았다. 한편 2010-2015년 한국원자력연구원은 과학기술부 연구과제를 지원받아 국산 Lu-177 DOTATATE를 개발하였다. 2018년부터 보건복지부 지원을 받아 치료불응성 및 진행성 신경내분비 종양환자에서 펩티드수용체 방사핵종치료의 비임상 및 임상 1상 시험을 진행 중이다.
아직 확립이 되지 않은 이슈는 옥트레오티드, 에베로리무스, 수니티닙, 간동맥화학/방사선색전술 등 기존 치료와 어떤 순서 또는 어떤 병합치료를 하는 것이 더 효과적인지, PRRT 4회 치료 후에 다시 진행할 때 어떤 간격으로 몇 회나 추가 치료를 할 것인지 등이 있다. G3 신경내분비종양 중 분화도가 좋은 Ki-67 <55% 이하의 환자를 대상으로 NETTER-2 다기관 3상 임상시험이 진행 중이다.
Lu-177, Y-90 등 베타선을 방출하거나 Ac-225, Bi-213 등 알파선을 방출하는 방사성동위원소를 표지한 펩티드수용체 치료는 고에너지 감마선을 방출하는 I-131과 달리 특별한 치료병실에서 입원할 필요가 없이 외래에서도 치료가 가능하여 핵의학치료를 활성화하는 데 유리한 조건이다. 특히 알파핵종 치료제의 경우 기존 베타핵종 Lu-177 DOTATATE 치료에 반응하지 않는 환자에서도 치료 효과가 뛰어나 핵의학 치료의 미래의 주역이 될 것이다[9].